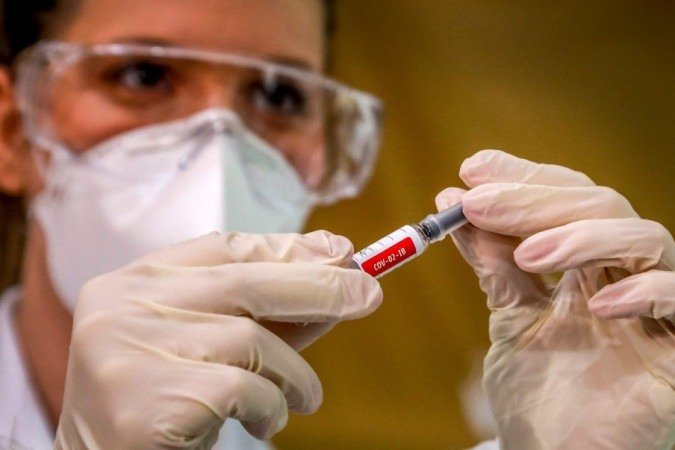
Em meio à pandemia do novo coronavírus, a humanidade parece ter encontrado uma missão comum: a busca por uma vacina eficaz contra a covid-19. Os pesquisadores precisaram se reinventar para ganhar agilidade na produção de um imunizante. Após estudos pré-clínicos, a tarefa nada simples envolve testes em seres humanos. Atualmente, o Brasil destaca-se por ser um local atraente para a realização dos ensaios, já que o país ainda convive com uma alta taxa de transmissão do novo coronavírus.
Os últimos dados do Ministério da Saúde mostram que, nas últimas 24 horas, o país registrou 16.158 casos da doença, a menor quantidade desde 8 de junho. E foram confirmadas mais 366 mortes, elevando o total de óbitos para 120.828. No total, já são mais de 3,8 milhões de casos no Brasil. Ainda ontem, o mundo ultrapassou a marca de 25 milhões de infectados. O Brasil é o segundo no ranking da covid-19, atrás dos Estados Unidos.
Já são quatro as imunizações autorizadas a serem testadas em voluntários brasileiros. Para chegar a essa etapa, porém, o caminho é árduo e passa pela Agência Nacional de Vigilância Sanitária (Anvisa), responsável por aprovar e acompanhar os estudos clínicos de vacinas dentro do país.
O órgão corre contra o relógio. Usualmente, a agência tem até 90 dias para se manifestar e aprovar ou não um estudo clínico. Nos últimos meses, contudo, o desafio tem sido completar a avaliação em até 72 horas após a formalização dos pedidos. “Mobilizamos um comitê instituído especificamente para tratar as demandas da covid-19. É um comitê multidisciplinar e, por isso, garante celeridade ao processo”, diz Gustavo Mendes, gerente-geral de Medicamentos e Produtos Biológicos da Anvisa.
Infectologista do Laboratório Exame, Maria Isabel de Moraes Pinto pondera que o momento pede agilidade, mas isso não é motivo para deixar de lado pontos importantes, como a vigilância de eventos adversos e a aprovação da Anvisa e do Comitê de Ética. “Mas podemos tentar abreviar algumas fases, sempre garantindo a transparência. Outras pessoas não ligadas ao desenvolvimento da vacina podem opinar e publicar os resultados das diferentes fases para que se possa ter uma vacina realmente segura”
A médica alerta, ainda, que, apesar de todos os esforços coletivos, o tempo para produção de cada vacina é diferente. “Já tivemos vacinas que levaram 60 anos para serem produzidas e temos vacinas que ainda não conseguimos desenvolver, como a do vírus do HIV”, exemplifica.
As vacinas testadas no Brasil possuem quatro tecnologias diferentes (veja quadro abaixo). Após analisar resultados de segurança e eficácia dos imunizantes, a Anvisa fará o controle da bula e da rotulagem de cada uma, que devem indicar como a vacina deve ser usada, quantas doses e os eventos adversos que podem causar nos indivíduos.
Tecnologia
Tanto para a vacina de Oxford, quanto para a chinesa CoronaVac, existe uma proposta de transferência de tecnologia para a produção do imunizante. No entanto, essa etapa pode ser mais complicada do que parece. “É preciso treinar as pessoas, ter os mesmos equipamentos, reproduzir as condições que existiam quando se fabricou a vacina lá fora”, detalha Mendes.
Segundo o gerente de medicamentos da Anvisa, a bula determinará qual a faixa etária coberta pela vacina. “Se tivermos dados somente de testes em pessoas de 18 a 55 anos, isso estará na bula e só essa faixa etária poderá ser vacinada”, aponta. Questionado pelo Correio, o Ministério da Saúde reforçou que os próprios testes feitos no Brasil vão indicar quais grupos devem receber o imunizante.
“Baseado nesses testes, no acompanhamento das evidências e das indicações, esses grupos prioritários serão definidos, porque nós temos que verificar a capacidade imunológica para cada faixa etária, cada característica genética da nossa população para que possamos, então, definir”, disse o secretário executivo da pasta, Élcio Franco. O gestor ainda destacou a criação de um grupo de trabalho com integrantes da comunidade científica para a definição dos públicos prioritários a serem imunizados. (Colaborou Sarah Teófilo)
Notícias pelo celular
Receba direto no celular as notícias mais recentes publicadas pelo Correio Braziliense. É de graça. Clique aqui e participe da comunidade do Correio, uma das inovações lançadas pelo WhatsApp.
Dê a sua opinião
O Correio tem um espaço na edição impressa para publicar a opinião dos leitores. As mensagens devem ter, no máximo, 10 linhas e incluir nome, endereço e telefone para o e-mail sredat.df@dabr.com.br.