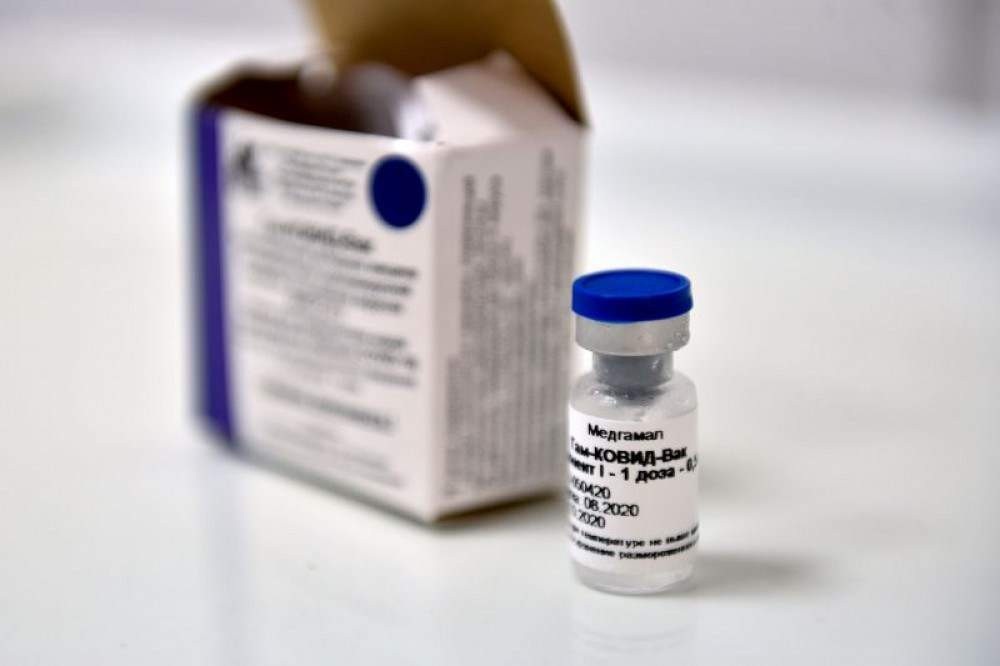
Acusada, pelos desenvolvedores da vacina russa Sputnik V, de ter espalhado “informações falsas e imprecisas intencionalmente” sobre o imunizante, a Agência Nacional de Vigilância Sanitária (Anvisa) rebateu as acusações nesta quinta-feira (29/4) e afirmou que a indicação da presença de adenovírus replicante na vacina constava em documentos entregues pelos próprios desenvolvedores.
A Anvisa ainda expôs um vídeo de uma das reuniões. “Iremos apresentar na tarde de hoje prova de que a Anvisa atuou com documentos enviados pelo próprio desenvolvedor, no qual este identificou a definição da presença do adenovírus replicante. Não há nessa instituição, Agência de Nacional de Vigilância Sanitária, nenhuma pessoa que tenha qualquer interesse ou júbilo em negar a importação de qualquer vacina”, afirmou o diretor-presidente da Anvisa, Antonio Barra Torres, durante a fala inicial.
Logo depois, o gerente-geral de medicamentos e produtos biológicos do órgão, Gustavo Mendes, explicou que a empresa atesta no próprio dossiê que o processo de fabricação das partículas RAD5-SCOV2 pode produzir partículas replicantes, que são aquelas que vão espalhar pelo corpo, o que não é esperado para uma vacina.
Além disso, o gerente pontua que a Sputnik V é composta por dois tipos de adenovírus, mas a empresa só apresentou a justificativa de não replicação para um deles.
Além de expor documentos que comprovam que as informações que indicam a presença de adenovírus replicante na vacina foram entregues pelos próprios desenvolvedores, o gerente também exibiu um vídeo de uma reunião com os representantes do laboratório russo, realizada em 23 de março.
Vídeo
No vídeo em questão (veja abaixo), uma especialista da Anvisa questiona a empresa russa o porquê de, uma vez que detectaram o adenovírus replicante durante a elaboração do imunizante, não terem voltado para o início dos estudos e optado por tecnologias sem efeitos homólogos. “Qual a justificativa que vocês têm para seguir com esse desenvolvimento de uma vacina que será usada em pessoas saudáveis?”
Em resposta, os representantes do laboratório disseram que, “para a produção da vacina, usaram uma linha de células caracterizada que pode ter seus defeitos”, e que concordam com os fiscais da Anvisa que podiam ter recomeçado o processo usando uma nova substância, mas que isso “ocuparia muito tempo” e que, então, optaram pela mesma substância que usaram no início.
Segundo Gustavo, as justificativas apresentadas não contemplam as questões apresentadas pelos técnicos da Anvisa. “São questões que envolvem a presença desse adenovírus replicante e de que forma esse adenovírus pode impactar na nossa saúde”, explica.
Veja trecho do vídeo no qual a Anvisa expõe a reunião com os representantes russos:
Credibilidade
Na fala de abertura do pronunciamento feito pela Anvisa, o diretor-presidente da Anvisa, Antonio Barra Torres, criticou as acusações feitas pelos fabricantes do imunizante russo. Segundo ele, a queixa feita pelo Fundo Russo de Investimento Direto (RDIF) e o Instituto Gamaleya “impacta na confiança e na credibilidade da autoridade sanitária do estado brasileiro”.
O presidente da agência ainda ressaltou que os ajustes em fármacos são necessários tendo em vista que o desenvolvimento destes é complexo e afirmou que a Anvisa se mantém de portas abertas para avaliar novos estudos e informações.
“O desenvolvimento é complexo e é de absoluta normalidade as necessidade de ajustes, portanto a Anvisa, no cumprimento do seu dever, está sempre receptiva para avaliar novos estudos e informações que podem ser enviadas no processo de autorização do uso emergencial ou em pedidos de importação”, completou.
*Estagiária sob a supervisão de Andreia Castro
Saiba Mais
-
![]() Brasil
Sputnik V: Governadores se reúnem com russos para mais informações
Brasil
Sputnik V: Governadores se reúnem com russos para mais informações
-
![]() Brasil
'Anvisa fez trabalho técnico e bem avaliado', diz Mourão sobre veto a Sputnik V
Brasil
'Anvisa fez trabalho técnico e bem avaliado', diz Mourão sobre veto a Sputnik V
-
![]() Brasil
Sputnik V: chanceler espera que Anvisa resolva pendência de modo 'satisfatório'
Brasil
Sputnik V: chanceler espera que Anvisa resolva pendência de modo 'satisfatório'
-
![]() Mundo
Desenvolvedores da vacina russa Sputnik V ameaçam processar Anvisa por difamação
Mundo
Desenvolvedores da vacina russa Sputnik V ameaçam processar Anvisa por difamação
Notícias pelo celular
Receba direto no celular as notícias mais recentes publicadas pelo Correio Braziliense. É de graça. Clique aqui e participe da comunidade do Correio, uma das inovações lançadas pelo WhatsApp.
Dê a sua opinião
O Correio tem um espaço na edição impressa para publicar a opinião dos leitores. As mensagens devem ter, no máximo, 10 linhas e incluir nome, endereço e telefone para o e-mail sredat.df@dabr.com.br.
 Brasil
Brasil
 Brasil
Brasil
 Brasil
Brasil
 Mundo
Mundo