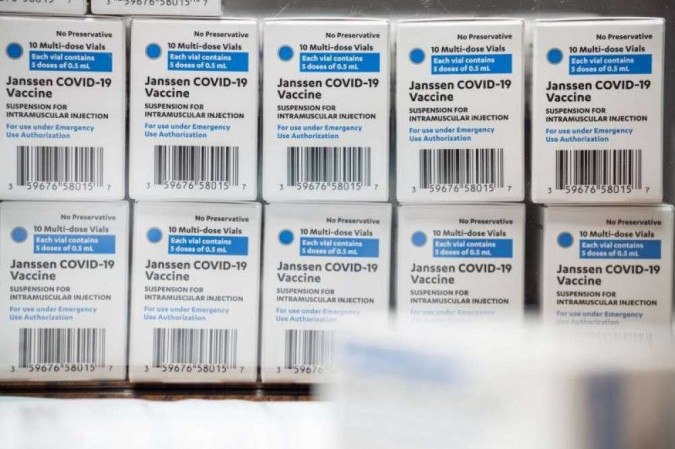
Representantes da Agência Nacional de Vigilância Sanitária (Anvisa) reuniram-se hoje (16/3), em Brasília, com representantes do laboratório Janssen, uma das empresas que fornecem vacinas ao governo brasileiro. O Ministério da Saúde anunciou ontem (15/3) a compra de 38 milhões de doses da farmacêutica.

Apesar da contratação, a vacina da Janssen ainda não teve registro aprovado no Brasil. O intuito da reunião, segundo a Anvisa, foi exatamente o de discutir e orientar a companhia para a formalização da solicitação de uso em caráter emergencial.
De acordo com a Anvisa, a Janssen ainda precisa complementar as informações fornecidas para análise pela equipe da agência.
Em nota, a Anvisa informa que ainda falta fechar as informações referentes à cadeia de produção da vacina que virá para o Brasil, que, pelas informações, não seria a mesma da Europa. "A cadeia produtiva envolve todas as fábricas envolvidas na produção da vacina, desde o insumo inicial até a vacina pronta para o uso", explica a nota da Anvisa.
Uma nova reunião deve ser realizada no dia 24 deste mês.
Notícias pelo celular
Receba direto no celular as notícias mais recentes publicadas pelo Correio Braziliense. É de graça. Clique aqui e participe da comunidade do Correio, uma das inovações lançadas pelo WhatsApp.
Dê a sua opinião
O Correio tem um espaço na edição impressa para publicar a opinião dos leitores. As mensagens devem ter, no máximo, 10 linhas e incluir nome, endereço e telefone para o e-mail sredat.df@dabr.com.br.