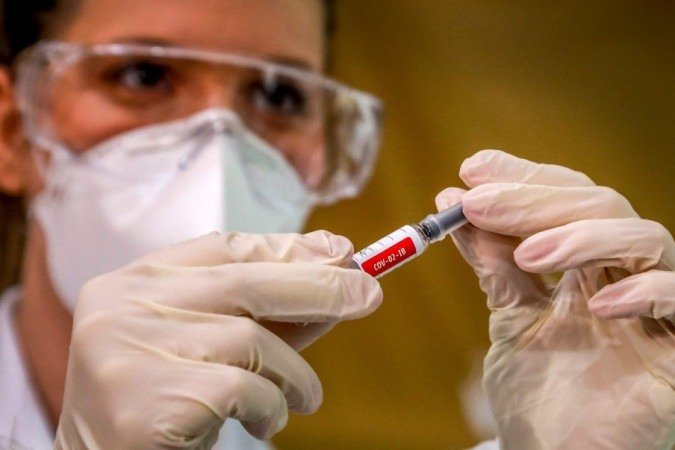
Muitos especialistas temem que Donald Trump pressione para que uma vacina contra o coronavírus seja autorizada nos Estados Unidos antes da eleição presidencial de 3 de novembro.
Os cientistas estimam que é improvável, embora não impossível, que os testes clínicos produzam resultados provisórios nos próximos dois meses.
Quais são os preparativos?
O Centro de Controle e Prevenção de Doenças (CDC) pediu "com urgência" na semana passada que os estados façam o que for necessário para que os centros de distribuição de uma futura vacina possam estar "totalmente operacionais em 1º de novembro de 2020".
O que Trump disse?
"Teremos uma vacina segura e eficaz este ano e, juntos, vamos aniquilar o vírus", disse o presidente Trump. Seu governo investiu 11 bilhões de dólares em vários projetos de vacinas, comprando antecipadamente centenas de milhões de doses, cuja produção já começou.
"Teremos centenas de milhões de vacinas disponíveis antes do final do ano", disse Paul Mango, um alto funcionário do Departamento de Saúde, na última sexta-feira.
Quais são as vacinas mais avançadas?
Dois fabricantes iniciaram o último estágio dos testes, a fase 3, nos Estados Unidos no dia 27 de julho e, segundo Mango, 15 mil voluntários dos 30 mil necessários já se inscreveram para participar.
Essas vacinas são administradas em duas doses, no caso da Pfizer com um intervalo de 21 dias e, no caso da Moderna, 28 dias. Ambas são baseados em uma tecnologia de RNA mensageiro que até agora não teve eficácia demonstrada.
Em estudos de fase 1 e/ou 2, com algumas dezenas de voluntários, as duas vacinas desencadearam uma resposta imunológica, mas isso não garante que elas protegerão contra a infecção.
Outra vacina, a britânica da Oxford e AstraZeneca, também está com testes de fase 3 em andamento em vários países e acabou de começar essa fase também nos Estados Unidos.
Como saberemos se uma vacina funciona?
É preciso esperar. Metade dos participantes recebe a vacina experimental e a outra metade, um placebo. Os participantes são acompanhados para que seja verificado se o grupo do placebo contrai mais coronavírus de forma natural e fica mais doente do que o grupo vacinado.
Os responsáveis pelos testes se concentraram em áreas onde a epidemia foi mais forte na esperança de que a vacina demonstre seus efeitos mais rapidamente.
O diretor do CDC, Robert Redfield, disse que, estatisticamente, 150 a 175 infecções no grupo do placebo em oposição a apenas algumas no grupo vacinado seriam suficientes para uma vacina demonstrar sua eficácia.
Para Anthony Fauci, diretor do Instituto Nacional de Alergias de Doenças Infecciosas, que gerencia os testes da vacina da Moderna, os primeiros resultados serão sem dúvida conhecidos por volta de novembro ou dezembro. Em entrevista à CNN na quinta-feira, ele afirmou ainda que, quanto a outubro, "é improvável, embora não impossível".
E o processo de autorização?
Tudo vai depender dos comitês de especialistas independentes que supervisionam os testes, disse à AFP Paul Offit, membro do conselho consultivo de vacinas da FDA, a agência reguladora de medicamentos dos EUA.
Esses comitês deverão considerar os dados provisórios suficientemente claros. Nesse caso, os fabricantes poderiam solicitar uma autorização de "emergência" do FDA.
A decisão ficará então nas mãos do diretor Stephen Hahn, que foi acusado de ceder à pressão política ao conceder autorizações de emergência para a hidroxicloroquina (agora revogada) e para o plasma sanguíneo de pessoas curadas de covid-19, apesar da falta de evidências rigorosas de efetividade.
Fauci, porém, insistiu que o papel de especialistas independentes no procedimento garantiria que o FDA não tomasse decisões políticas. "Podemos ter confiança no que o FDA vai dizer", assegurou.
Pressões políticas?
A porta-voz da Casa Branca, Kayleigh McEnany, disse na quinta-feira que "ninguém está pressionando o FDA para nada". Mas permanece a preocupação com os padrões científicos, que são menores para autorizações de emergência do que para autorizações normais.
"Como justificar uma avaliação abaixo do padrão ou inferior para algo que seria injetado em dezenas de milhões, talvez centenas de milhões de americanos?", questionou especialista em vacinas Peter Hotez, professor do Baylor College, no Twitter.
O calendário anunciado "sugere que pressão política, e não ciência e dados, podem estar conduzindo esta decisão", disse à AFP o médico Ezekiel Emanuel, da Universidade da Pensilvânia, que assessora o candidato presidencial democrata Joe Biden.
"Ainda estou preocupado com uma surpresa em outubro", resumiu Paul Offit, diretor do Centro de Educação de Vacinas do Hospital Infantil da Filadélfia.
Notícias pelo celular
Receba direto no celular as notícias mais recentes publicadas pelo Correio Braziliense. É de graça. Clique aqui e participe da comunidade do Correio, uma das inovações lançadas pelo WhatsApp.
Dê a sua opinião
O Correio tem um espaço na edição impressa para publicar a opinião dos leitores. As mensagens devem ter, no máximo, 10 linhas e incluir nome, endereço e telefone para o e-mail sredat.df@dabr.com.br.