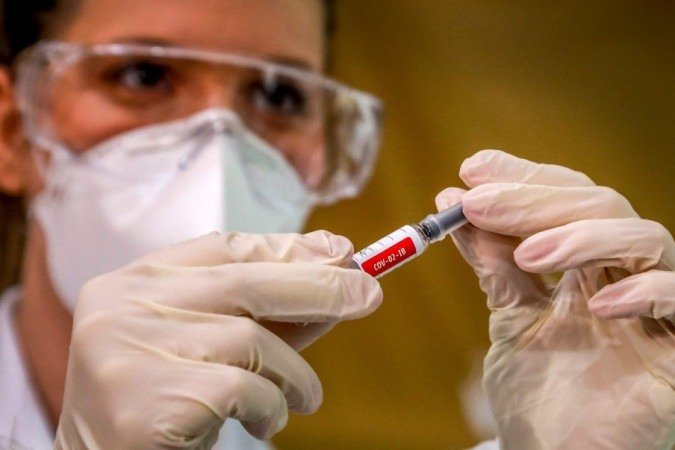
Mais uma vacina contra a covid-19 recebeu o aval da Agência Nacional de Vigilância Sanitária (Anvisa) para conduzir ensaios clínicos no Brasil. A decisão saiu no Diário Oficial da União (DOU) desta terça-feira (18/8) e entra em vigor na data de publicação. Batizado de Ad26.COV2.S, o imunizante é desenvolvido pela empresa Janssen-Cilag Farmacêutica. A previsão é que o estudo se inicie em setembro e que sete mil voluntários de sete estados brasileiros sejam recrutados.
De acordo com informações do site da agência, o ensaio clínico aprovado é para a fase 3: "randomizado, duplo cego, controlado por placebo, para avaliar a eficácia e a segurança de Ad26.COV2.S na prevenção de covid-19 mediada por Sars-CoV-2 em adultos com 18 anos ou mais". O texto ainda informa que a vacina será aplicada em dose única ou placebo para o teste.
Ao todo o estudo deverá contar com até 60 mil voluntários, sete mil desse total devem ser do Brasil. São Paulo, Rio Grande do Sul, Rio de Janeiro, Paraná, Minas Gerais, Bahia e Rio Grande do Norte são os estados que participam desta fase da pesquisa. O recrutamento dos voluntários é responsabilidade dos centros que conduzem a pesquisa.
Saiba Mais
-
![]() Cidades DF
Voluntários contam por que se inscreveram para testar vacina contra covid
Cidades DF
Voluntários contam por que se inscreveram para testar vacina contra covid
-
Cidades DF Secretaria de Saúde convoca jovens para vacinação contra HPV
-
![]() Ciência e Saúde
Primeira vacina contra a covid patenteada poderá ser testada no Brasil
Ciência e Saúde
Primeira vacina contra a covid patenteada poderá ser testada no Brasil
-
![]() Mundo
Esforços contra coronavírus precisam ser conjuntos, diz OMS
Mundo
Esforços contra coronavírus precisam ser conjuntos, diz OMS
Antes de aprovar o ensaio clínico, a Anvisa realizou reuniões com a equipe da Janssen, para alinhar todos os requisitos técnicos necessários para a condução dos testes. "Os dados que embasaram a autorização da Anvisa incluíram estudos não clínicos com a vacina e dados não clínicos e clínicos acumulados de outras vacinas que utilizam a mesma plataforma Ad26", informou o texto publicado.
Notícias pelo celular
Receba direto no celular as notícias mais recentes publicadas pelo Correio Braziliense. É de graça. Clique aqui e participe da comunidade do Correio, uma das inovações lançadas pelo WhatsApp.
Dê a sua opinião
O Correio tem um espaço na edição impressa para publicar a opinião dos leitores. As mensagens devem ter, no máximo, 10 linhas e incluir nome, endereço e telefone para o e-mail sredat.df@dabr.com.br.
 Cidades DF
Cidades DF
 Ciência e Saúde
Ciência e Saúde
 Mundo
Mundo