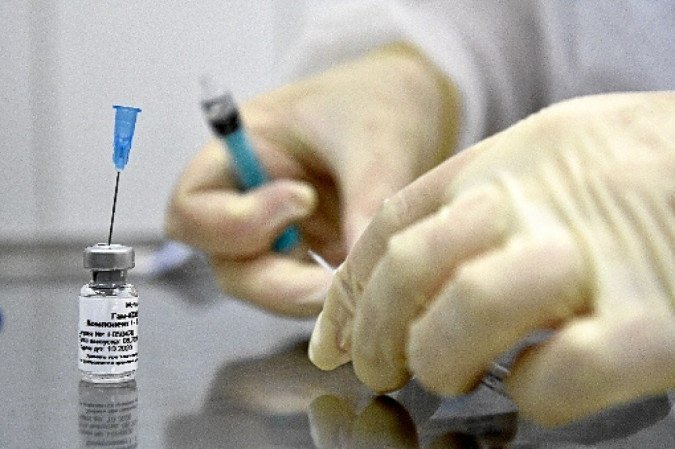
O Distrito Federal, que é polo de teste de uma vacina contra a covid-19, receberá um segundo ensaio com moradores voluntários a partir outubro e ainda pode vir a produzir uma outra imunização. O ex-deputado Rogério Rosso, Diretor de Negócios Internacionais da União Química, tem investido em um acordo com o governo russo para a produção da Sputnik V, a primeira vacina a ser registrada para uso amplo no mundo.
Os termos da negociação são confidenciais e técnicos da empresa discutem o tema em Moscou. O próprio ex-deputado deve ir ao país nas próximas semanas, confiando na eficiência do produto. Mas, no Brasil, pouco se sabe sobre essa vacina divulgada com empolgação na Rússia.
Uma das principais críticas de cientistas é o fato de que o anúncio do registro foi feito antes dos estudos de fase 3. Essa etapa é considerada fundamental para definir se o produto é seguro e eficaz em uma grande quantidade de pessoas, e antecede a fase de produção e disponibilização à população. A fase 3 da Sputnik V começou recentemente, em 9 de setembro, segundo o Ministério da Saúde da Rússia, cerca de um mês após o anúncio do desenvolvimento.
A efeito de comparação, a fase 3 da vacina CoronaVac teve início em julho no Brasil e no começo de agosto no DF, com aplicação do produto em profissionais da saúde voluntários. Atualmente, quatro imunizações nessa etapa de pesquisa estão sendo aplicadas em brasileiros. Todas elas passaram por avaliação e aprovação da Agência Nacional de Vigilância Sanitária (Anvisa) para os testes.
No caso da Sputnik V, a Anvisa esclarece que, como o desenvolvimento clínico dessa vacina foi conduzido totalmente fora do Brasil, não cabe à agência aprovar os estudos. “Porém, é necessário o cumprimento dos devidos procedimentos para registro da vacina”, informou o órgão, em nota.
Para acompanhar o andamento de um possível registro, a Anvisa tem se reunido com membros do governo do Paraná. Isso porque o estado enviou um protocolo de ensaio clínico e busca aprovação da agência para conduzir testes de fase 3. O governo afirmou que analisou os resultados das etapas anteriores e avaliou que “existe uma boa taxa de confiabilidade nessa vacina” e que “a confiabilidade é bastante ampla”, conforme divulgado na página oficial do Estado.
Notícias pelo celular
Receba direto no celular as notícias mais recentes publicadas pelo Correio Braziliense. É de graça. Clique aqui e participe da comunidade do Correio, uma das inovações lançadas pelo WhatsApp.
Dê a sua opinião
O Correio tem um espaço na edição impressa para publicar a opinião dos leitores. As mensagens devem ter, no máximo, 10 linhas e incluir nome, endereço e telefone para o e-mail sredat.df@dabr.com.br.