O menino Roo, de sete anos, ficou doente no início do ano passado. Sintomas como sua perda de peso e muita sede levaram seus médicos e seus pais a recear que ele pudesse ter um tumor no cérebro.
Mas as investigações concluíram que ele havia sido acidentalmente envenenado com uma overdose de vitamina D, prescrita para tratar das suas dores crescentes.
A concentração do frasco de vitamina D3 em gotas consumido por Roo era cerca de sete vezes maior do que o normal. Ele fazia parte de um dentre dois lotes com defeito de produção que foram distribuídos no Reino Unido.
A dosagem levou Roo a sofrer lesão renal aguda e um especialista contou à BBC que a criança teria morrido, se tivesse levado o tratamento prescrito até o fim.

A vitamina D é um nutriente vital que regula o cálcio e o fosfato, mantendo a saúde dos ossos, dentes e músculos. Milhões de adultos a consomem na forma de suplementos, que são vendidos nas farmácias.
Mas, no Reino Unido, a vitamina D em dosagem mais alta, receitada pelos médicos, ainda é classificada como suplemento alimentar e não é regulamentada pelo órgão regulador britânico, a MHRA (Agência Reguladora de Remédios e Produtos para Assistência Médica, na sigla em inglês).
O órgão britânico responsável pelo acompanhamento das vitaminas e suplementos alimentares é a Agência de Padrões Alimentares (FSA, na sigla em inglês).
A MHRA afirma que trabalha em conjunto com a FSA para manter a segurança do público. Mas um especialista contou à BBC que o órgão regulador de remédios deveria buscar mudanças na forma de regulamentação dos suplementos vitamínicos.
No Brasil, o órgão responsável pela fiscalização tanto dos medicamentos, quanto dos suplementos alimentares (incluindo os vitamínicos), é a Agência Nacional de Vigilância Sanitária (Anvisa).
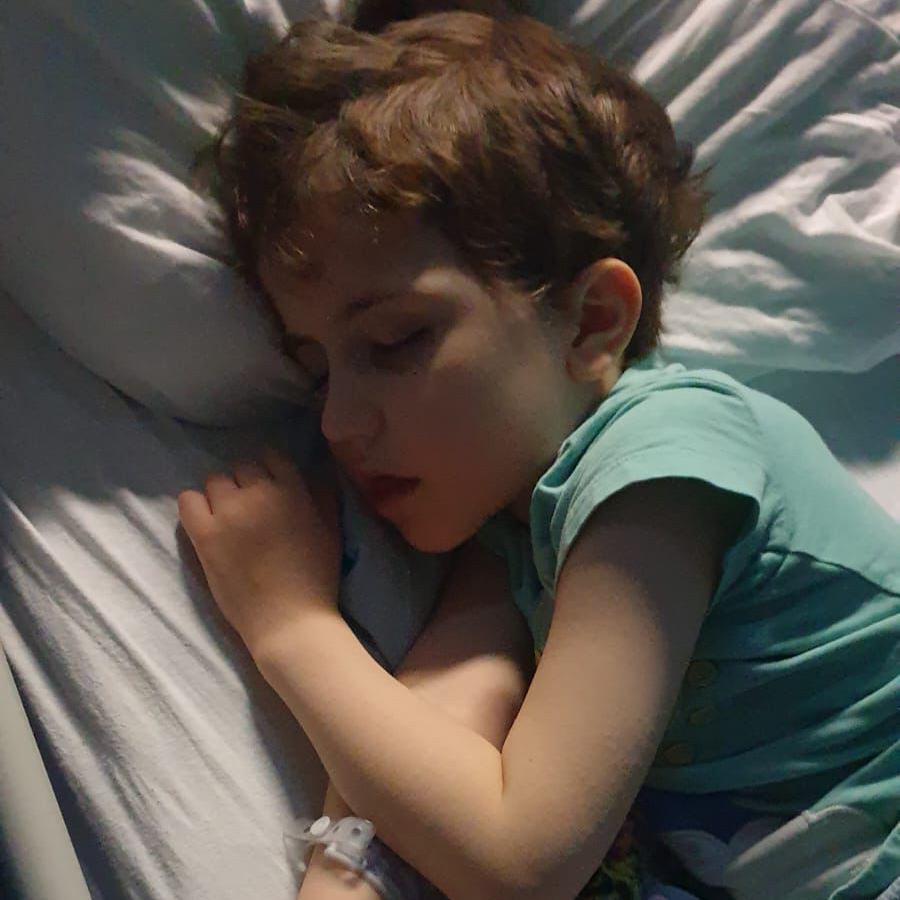
Em dezembro de 2024, Roo recebeu prescrição de uma alta dose de vitamina D3 em gotas por 12 semanas, para tentar diminuir a sua intensa dor nas pernas.
A receita veio após o menino ter sido encaminhado para a pediatria do hospital Crosshouse, perto de sua casa em Kilmarnock, no condado de Ayrshire (sudoeste da Escócia).
Exames de sangue demonstraram que ele estava bem e saudável, exceto por um nível levemente mais baixo de vitamina D. Ele recebeu suplementos contendo vitamina D3, também conhecida como colecalciferol, para elevar o nível da substância no sangue.
Nas semanas seguintes, Roo ficou sonolento e sem apetite. Ele começou a perder peso e beber água "como se estivesse no deserto", segundo sua mãe, Carys Hobbs-Sargeant.
Roo também teve crises de vômito durante todo o mês de janeiro e dificuldades para comer.
"Ele estava muito doente", conta Carys. "Ele perdeu mais de 10% do peso do corpo em seis semanas. Tinha os olhos enormes e estava tão cansado que simplesmente não conseguia comer."
Roo se consultou novamente com o pediatra e foi imediatamente internado.
Os exames de sangue iniciais demonstraram que Roo tinha uma lesão renal aguda. Seus rins estavam extremamente desidratados e os médicos começaram a busca a causa.
Inicialmente, eles não se preocuparam com a receita de vitamina D, pois o menino havia cumprido apenas dois terços do tratamento com a dose recomendada. Mas sua condição continuou a se deteriorar.
"Ele teve hipercalcemia e os médicos ficaram muito preocupados com esse nível tão alto de cálcio no sangue", conta a mãe.
"Eles examinavam se poderia ser um tumor cerebral e estávamos meio que nos preparando para que ele fizesse uma ressonância magnética do cérebro."
O misterioso caso de Roo também foi analisado por equipes do Hospital Real Infantil de Glasgow, na Escócia. E uma ligação telefônica casual com um endocrinologista forneceu a peça que faltava no quebra-cabeça.
Um colega de Manchester, na Inglaterra, havia perguntado se ele sabia de algum "lote ruim" de vitamina D3. E, com os detalhes do lote, a equipe que cuidava de Roo conseguiu identificar o frasco que o menino ainda usava para tomar as gotas todos os dias.
"Deduzimos dali que era o seu corpo fazendo algo estranho porque, basicamente, ele foi envenenado por aquele lote ruim", conta Hobbs-Sargeant.
"Você se sente aliviada, sortuda e furiosa ao mesmo tempo, por não ser câncer, mas por aquilo ter acontecido com ele. É basicamente envenenamento."
O frasco de vitamina de Roo foi identificado como pertencente a um dentre dois lotes com defeito de suplementos Aactive D3 da empresa TriOn Pharma, que foram distribuídos pelo Reino Unido.
O suplemento tinha concentração sete vezes maior do que o normal.
Os lotes irregulares sofreram recall da FSA no dia 9 de janeiro, mas a sua filial escocesa (a FSS, na sigla em inglês), responsável pelo recall local, declarou que o alerta não chegou aos departamentos corretos.
A investigação também descobriu que a farmácia de Ayrshire que forneceu o frasco só recebeu o e-mail sobre o recall do fabricante cerca de três meses depois do envio.
Os alertas sobre remédios, enviados pela MHRA, teriam seguido para a caixa de entrada clínica de alta prioridade das farmácias, para que fossem lidos imediatamente.

O professor Stuart Ralston, da Universidade de Edimburgo, na Escócia, é ex-presidente da Comissão de Remédios Humanos da MHRA. Ele afirma que o caso de Roo exemplifica por que o mesmo organismo responsável pelos remédios deveria considerar a possibilidade de assumir a regulamentação dos suplementos vitamínicos.
"Estima-se que o produto tivesse sete vezes a quantidade de vitamina D indicada no rótulo", comenta ele. "Eu não havia visto um caso destes em mais de 40 anos de carreira."
"O tratamento prescrito era de 12 semanas. Se ele tivesse seguido até o fim, seriam 3,5 milhões de unidades, o que por sorte não aconteceu. Porque, se ele tivesse feito, sem dúvida teria morrido."
Ralston afirma que, se o suplemento fosse regulamentado como remédio, o médico de Roo provavelmente teria recebido um alerta urgente.
A MHRA declarou que a regulamentação de suplementos alimentares é atribuição da FSA e que as duas agências trabalham juntas para manter a segurança dos consumidores.
A FSS afirma que trabalha em conjunto com a Agência de Padrões Alimentares e as autoridades locais para garantir a comunicação correta dos recalls de produtos.
O governo escocês informou Hobbs-Sargeant que encaminhou a questão da regulamentação e dos recalls de suplementos para o Departamento de Saúde e Assistência Social do Reino Unido.

Um mês antes de Roo começar seu tratamento com a vitamina D3 em gotas, Kayan Khan, de Sheffield, na Inglaterra, também recebeu prescrição da mesma marca de suplementos.
Kayan tem 13 anos e enfrenta diversas condições médicas complexas, incluindo doença renal crônica. E o tratamento de oito semanas com vitamina D receitado pelo seu médico estava de acordo com as recomendações.
Em fevereiro de 2025, o menino foi internado no hospital em Sheffield, com altos níveis de cálcio e redução da função renal.
Uma carta enviada pela Fundação do Serviço Nacional de Saúde britânico (NHS, na sigla em inglês) do Hospital Infantil de Sheffield para a mãe de Kayan, Alaina, informou que os médicos tiveram dificuldade para controlar seus níveis de cálcio e concluíram que ele estava intoxicado com vitamina D em níveis "muito acima do esperado com a suplementação padrão".
Ela não guardou o frasco da vitamina em gotas, de forma que não foi possível confirmar exatamente o número de lote. Mas a carta afirmava que a "explicação lógica" para o seu nível de toxicidade era a ingestão elevada de vitamina D.
Mais uma vez, a notícia do recall da FSA não chegou, mesmo tendo sido transmitida para os médicos do hospital e para a as farmácias locais. A mãe conta que só ficou sabendo do recall em abril de 2025.
Kayan sofreu deterioração significativa da sua função renal e, embora já tenha se recuperado levemente, ele pode precisar de um transplante no futuro.
"Como mãe, fiquei desamparada", lamenta ela. "Não posso deixar de sentir que, por oito semanas, eu vinha lentamente envenenando meu filho."
O diretor médico executivo da Fundação do NHS do Hospital Infantil de Sheffield, Jeff Perring, declarou que a prática padrão é pedir aos médicos que prescrevam a medicação, seguindo procedimentos rigorosos para informar aos pacientes e às famílias sobre recalls de medicamentos receitados diretamente.
O fabricante das gotas, a empresa TriOn Pharma, afirmou ter iniciado o recall imediatamente após a identificação do problema e notificado a FSA e a MHRA, seguindo os procedimentos estabelecidos.
"As notificações do recall foram enviadas a todos os consumidores diretos por meio de canais estabelecidos para comunicação em toda a cadeia de abastecimento", afirma a empresa. "Continuamos trabalhando com as autoridades para garantir a segurança dos pacientes."

Os níveis de vitamina D de Roo levaram cerca de um ano para voltar à faixa de segurança. E Carys Hobbs-Sargeant conta que ainda não se sabe ao certo quais serão os efeitos a longo prazo.
"Ele deixou de ser um aluno de uma escola florestal, em ambiente externo, e agora precisa de uma cadeira de rodas para sair por distâncias mais longas", lamenta ela.
"Ele não voltou imediatamente a ser quem ele era e ainda enfrenta dificuldades todos os dias."
- Vitamina D: o que se sabe e o que falta saber sobre suplementos, benefícios e riscos
- Como chatbot de IA descobriu condição rara de mulher após anos de diagnósticos errados
- 'A voz da filha que perdi está sendo honrada': as tragédias que o novo estatuto do paciente pretende evitar
- A razão pela qual tomar vitamina D sem receita médica pode não ser boa ideia
- Ela ficava tonta e só conseguia fazer o mínimo com os filhos, e o médico falou que era 'apenas cansaço de mãe' — não era
- 5 coisas que todos deveriam saber antes de tomar suplementos alimentares