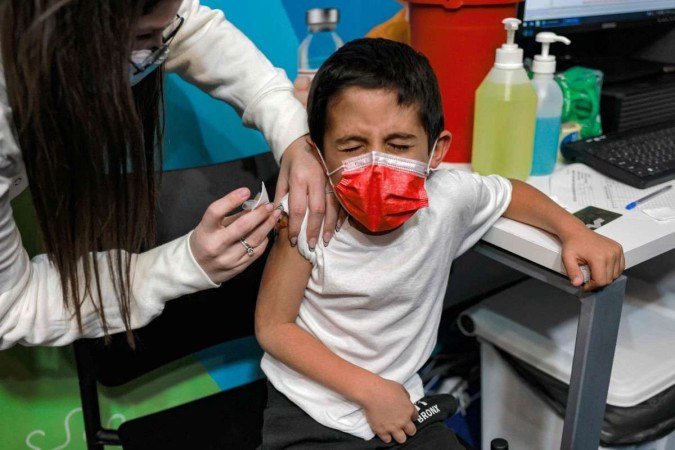
A Agência Nacional de Vigilância Sanitária (Anvisa) aprovou, ontem, o uso da vacina da Pfizer contra a covid-19 para crianças de cinco a 11 anos. A conclusão da área técnica da agência é de que os benefícios do imunizante para essa faixa etária superam os riscos.
Apesar de ter o mesmo princípio ativo do fármaco já comprado pelo Brasil e aplicado em pessoas com mais de 12 anos, a formulação da vacina aprovada para a população pediátrica é diferente — o que levará à aquisição de novos lotes pelo Ministério da Saúde. A intenção da pasta é incluir esse público-alvo na campanha de imunização contra a covid-19.
Durante a reunião que aprovou a vacina, os técnicos da Anvisa explicaram que uma das diversas diferenças entre os imunizantes da farmacêutica está na dosagem, que é menor para crianças. Além disso, as substâncias que compõem o imunizante são diferentes, assim como as condições para armazenamento e os frascos para envazamento. A Anvisa ressaltou que será necessário elaborar material e treinamento para evitar erros na aplicação.
Saiba Mais
-
![]() Brasil
Grupo neonazista que incitava ódio e racismo na internet é preso pela Polícia Civil
Brasil
Grupo neonazista que incitava ódio e racismo na internet é preso pela Polícia Civil
-
![]() Brasil
Inep divulga lista de estudantes regulares no Enade
Brasil
Inep divulga lista de estudantes regulares no Enade
-
![]() Brasil
Confira os resultados da Quina 5732 e da Timemania 1726 desta quinta (16/12)
Brasil
Confira os resultados da Quina 5732 e da Timemania 1726 desta quinta (16/12)
-
![]() Brasil
Homem suspeito de estuprar enteada de 17 em frente da filha de 1 ano é preso
Brasil
Homem suspeito de estuprar enteada de 17 em frente da filha de 1 ano é preso
Nada neste ano
Apesar da decisão da Anvisa, o ministro da Saúde, Marcelo Queiroga, afirmou que a vacinação de crianças contra a covid-19 não começa neste ano. "Quantos dias faltam para (acabar) 2021? Vocês acham que têm? Quanto tempo a Anvisa demorou para dar um posicionamento acerca dessas doses? É preciso ser feita uma análise. A Anvisa é uma avaliação. A avaliação que é feita pela Câmara Técnica do ministério é outra", disse.
De acordo com o ministro, antes do início da vacinação das crianças haverá uma "discussão ampla" que inclui a sociedade civil, os cientistas e o Conselho Nacional de Justiça (CNJ). A pasta não reservou doses para aplicar no grupo de cinco a 11 anos.
Este público, aliás, pode ter mais uma opção de vacina além da Pfizer. Isso porque, na última quarta-feira, o Instituto Butantan fez um novo pedido para que a Anvisa avalie a recomendação da CoronaVac para uma faixa de idade entre três e 17 anos.
Em agosto, a Diretoria Colegiada da Anvisa considerou, por unanimidade, não ser seguro aprovar o uso do imunizante desenvolvido pela Sinovac para aplicação edm crianças e adolescentes "por causa da limitação de dados dos estudos apresentados naquele momento".
Notícias pelo celular
Receba direto no celular as notícias mais recentes publicadas pelo Correio Braziliense. É de graça. Clique aqui e participe da comunidade do Correio, uma das inovações lançadas pelo WhatsApp.
Dê a sua opinião
O Correio tem um espaço na edição impressa para publicar a opinião dos leitores. As mensagens devem ter, no máximo, 10 linhas e incluir nome, endereço e telefone para o e-mail sredat.df@dabr.com.br.
 Brasil
Brasil
 Brasil
Brasil
 Brasil
Brasil
 Brasil
Brasil