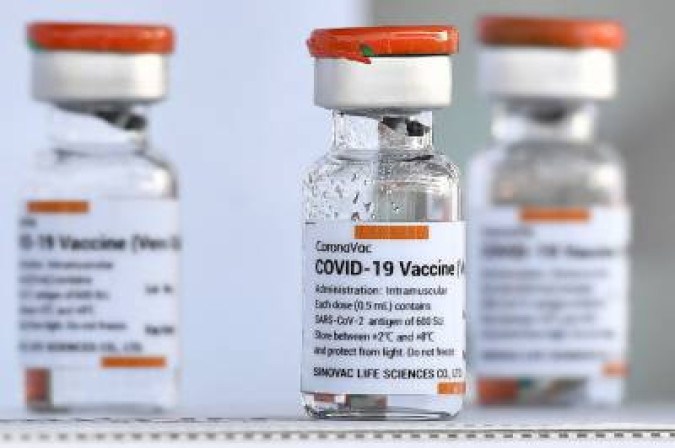
Após promover uma reunião com representantes do Instituto Butantan e especialistas representantes de sociedades médicas do Brasil para debater o pedido de autorização do uso da vacina CoronaVac em crianças, os técnicos da Agência Nacional de Vigilância Sanitária (Anvisa) concluíram, nesta terça-feira (21/12), que ainda faltam informações para que a equipe avalie o pedido feito pelo instituto paulista.
Dessa forma, a agência enviará ao Butatan uma série de questionamentos que ainda não estão presentes no processo e que impedem a conclusão da análise da Anvisa sobre a vacina. Com isso, o prazo de 30 dias para análise do pedido do Butantan fica pausado até que o instituto responda as dúvidas da Anvisa.
"Após a reunião com os especialistas e considerando a necessidade de maiores informações, a equipe conclui pela necessidade de emissão de exigência ao Butantan para a apresentação de informações ausentes no processo", informou a Anvisa em nota.
A reunião, que foi dividida em dois momentos, ouviu representantes de sociedade médicas, em uma segunda parte, após o Butantan apresentar os dados disponíveis sobre os estudos do uso da CoronaVac em crianças.
Os especialistas externos avaliaram que "há lacunas importantes nos dados apresentados pelo Butantan que ainda impedem afirmar de forma científica o grau de imunidade gerado nas crianças e adolescentes".
Em agosto, a Diretoria Colegiada da Anvisa, negou, por unanimidade, o mesmo pedido “por causa da limitação de dados dos estudos apresentados naquele momento". Na avaliação do técnicos, "praticamente não houve mudança em relação aos dados" do pedido indeferido e o pedido mais recente.
Pfizer
Na última semana, o órgão regulador brasileiro aprovou a vacina da Pfizer para criança de 5 a 11 anos. No entanto, até o momento, o Ministério da Saúde não indicou que indicará o imunizante para o público pediátrico.
A aprovação ocorreu após os diretores e servidores da agência terem sofrido ameaças diante da possibilidade da aprovação do imunizante para o público pediátrico. O ambiente hostil se intensificou quando de fato a aprovação foi realizada. Os servidores têm sofrido, desde então, os mais diversos ataques e represálias por parte do governo de Jair Bolsonaro e aliados.
Saiba Mais
-
![]() Brasil
Confira os resultados da Quina 5736 e Dupla Sena 2313 desta terça (21/12)
Brasil
Confira os resultados da Quina 5736 e Dupla Sena 2313 desta terça (21/12)
-
![]() Brasil
STF determina mais 90 dias para repasse que garante Internet às escolas públicas
Brasil
STF determina mais 90 dias para repasse que garante Internet às escolas públicas
-
![]() Brasil
Chuvas voltam a prejudicar diversas cidades da Bahia
Brasil
Chuvas voltam a prejudicar diversas cidades da Bahia
-
![]() Brasil
Por que as reuniões familiares no Natal podem se transformar em ambientes tóxicos?
Brasil
Por que as reuniões familiares no Natal podem se transformar em ambientes tóxicos?
Notícias pelo celular
Receba direto no celular as notícias mais recentes publicadas pelo Correio Braziliense. É de graça. Clique aqui e participe da comunidade do Correio, uma das inovações lançadas pelo WhatsApp.
Dê a sua opinião
O Correio tem um espaço na edição impressa para publicar a opinião dos leitores. As mensagens devem ter, no máximo, 10 linhas e incluir nome, endereço e telefone para o e-mail sredat.df@dabr.com.br.
 Brasil
Brasil
 Brasil
Brasil
 Brasil
Brasil
 Brasil
Brasil