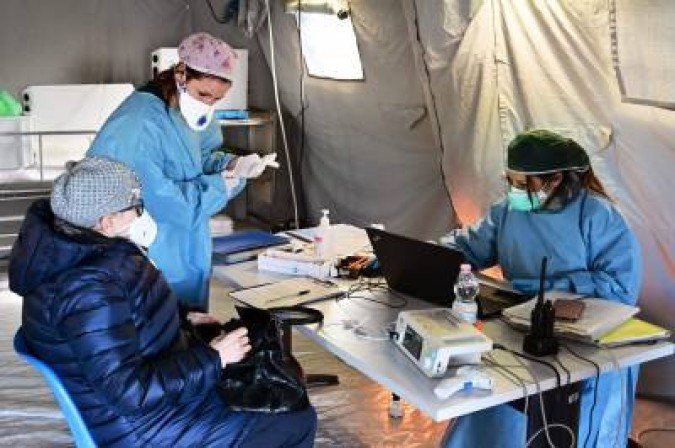
Um medicamento oral do laboratório norte-americano Pfizer reduziu em 89% o risco de hospitalização ou morte em pacientes adultos de covid-19 com risco elevado de doença grave. Essa é a segunda pílula anunciada para combater a enfermidade causada pelo Sars-CoV-2 — a farmacêutica MSD, também dos EUA, lançou, no mês passado, o molnupiravir, desenvolvido inicialmente como antigripal.
Desenvolvido especificamente para lutar contra a covid, o Paxlovid, da Pfizer, obteve resultados tão bons no teste clínico intermediário que o laboratório informou que vai interromper os exames e enviar os dados para a Agência de Alimentos e Medicamentos (FDA), dos Estados Unidos, o mais rápido possível, para obter a autorização de uso emergencial. Os dados divulgados fazem parte de um comunicado da empresa, ainda não foram divulgados em uma revista científica, o que implica em uma revisão por pares.
Diretor executivo da Pfizer, Albert Bourla disse à CNN que espera que o pedido de autorização possa chegar antes de 25 de novembro. "A notícia de hoje é uma mudança autêntica nos esforços globais para deter a devastação desta pandemia", afirmou. "Esses dados sugerem que nosso candidato a antiviral oral, se aprovado ou autorizado pelas agências reguladoras, tem o potencial de salvar a vida dos pacientes, reduzir a gravidade das infecções por covid-19 e evitar até nove em cada 10 hospitalizações", acrescentou. Segundo o presidente americano, Joe Biden, o governo reservou milhões de doses antes da decisão da FDA. A pílula, diz, constituirá "outra ferramenta em nossa caixa de ferramentas para proteger a população dos piores resultados da covid-19".
A principal análise do teste avaliou dados de 1.219 adultos na América do Norte, América do Sul, Europa, África e Ásia. Nos dias posteriores ao surgimento dos sintomas, alguns deles receberam o fármaco experimental e outros, um placebo, durante cinco dias, a cada 12 horas. "A análise intermediária programada mostrou uma redução de 89% no risco de hospitalização relacionada com a covid-19 ou morte por qualquer causa, em comparação com o placebo em pacientes tratados dentro dos três dias posteriores ao início dos sintomas", afirmou a Pfizer. Dez pessoas que tomaram o placebo morreram, enquanto nenhuma faleceu entre as que tomaram o medicamento.
Replicação bloqueada
A Pfizer começou a desenvolver o medicamento anticovid em março de 2020, o primeiro pensado especificamente contra o coronavírus. O produto é conhecido como um inibidor de protease e demonstrou, em exames de laboratório, que bloqueia o sistema de replicação do vírus. Se funcionar, provavelmente será eficaz apenas nos estágios iniciais da infecção, pois, quando a covid progride para uma doença grave, o vírus para de se replicar em grande medida, e os pacientes apresentam uma resposta imunológica mais ativa.
Desde o início da pandemia se busca uma pílula simples para combater o coronavírus, mas, até o momento, as terapias anticovid — como os anticorpos monoclonais e o remdesivir, do laboratório Gilead, com uso autorizado na União Europeia com o nome de Veklury — são aplicadas por via intravenosa. Vários laboratórios trabalham em antivirais orais que tentam imitar o que o medicamento Tamiflu faz na ação contra a gripe e que evitaria a evolução da doença para etapas de gravidade.
O Reino Unido, um dos mais afetados pela pandemia, aprovou, na quinta-feira, o uso do antiviral molnupiravir, da MSD, para tratar pacientes que sofrem da doença leve a moderada. "Esse é um dia histórico para nosso país, porque o Reino Unido é agora o primeiro do mundo a aprovar um antiviral contra a covid-19 que pode ser tomado em casa", afirmou o ministro da Saúde, Sajid Javid, em um comunicado. "Isto mudará a situação para os mais vulneráveis e os imunodeprimidos, que, em breve, poderão receber o tratamento revolucionário", acrescentou.
Saiba Mais
-
![]() Ciência e Saúde
Governo australiano cria campanha de encorajamento à masturbação
Ciência e Saúde
Governo australiano cria campanha de encorajamento à masturbação
-
![]() Ciência e Saúde
Retomada de eventos sociais requer cobertura vacinal de 80%
Ciência e Saúde
Retomada de eventos sociais requer cobertura vacinal de 80%
-
![]() Ciência e Saúde
Antiviral da Pfizer reduz em 89% risco de covid grave, diz empresa
Ciência e Saúde
Antiviral da Pfizer reduz em 89% risco de covid grave, diz empresa
-
![]() Ciência e Saúde
Por que este texto pode mudar seu cérebro — as descobertas da neurociência sobre a leitura
Ciência e Saúde
Por que este texto pode mudar seu cérebro — as descobertas da neurociência sobre a leitura
Notícias pelo celular
Receba direto no celular as notícias mais recentes publicadas pelo Correio Braziliense. É de graça. Clique aqui e participe da comunidade do Correio, uma das inovações lançadas pelo WhatsApp.
Dê a sua opinião
O Correio tem um espaço na edição impressa para publicar a opinião dos leitores. As mensagens devem ter, no máximo, 10 linhas e incluir nome, endereço e telefone para o e-mail sredat.df@dabr.com.br.
Testes com versão oral do remdesivir
Ao lado do molnupiravir, o remdesivir é, atualmente, o único medicamento antiviral aprovado para o tratamento de covid-19, mas deve ser administrado por via intravenosa. Para alcançar melhor os pacientes ambulatoriais logo após a infecção, o laboratório Gilead Sciences fez parceria com pesquisadores do Centro de Pesquisa de Antivirais Translacionais da Universidade Estadual da Georgia, nos EUA, para testar uma versão modificada do medicamento, em forma de comprimido.
Esse composto modificado "foi altamente eficaz na supressão da replicação e transmissão do Sars-CoV-2 em animais quando administrado por via oral", disseram os autores em um estudo publicado on-line na revista Nature Communications. De acordo com o texto, o medicamento "pode ser inovador na melhoria do acesso do paciente ao tratamento logo após a infecção".
"Quando tomado por via oral, o medicamento é rapidamente convertido na mesma substância bioativa que o remdesivir intravenoso, proporcionando todos os benefícios da versão aprovada pelo FDA, sem sua limitação de que os pacientes devem ser hospitalizados antes de iniciar o tratamento", diz Richard Plemper, autor sênior do estudo e diretor do Centro de Pesquisa de Antivirais Translacionais.
Os testes foram feitos com furões. Descobriu-se também que a droga era muito potente contra variantes do coronavírus recentemente surgidas, bloqueando efetivamente a propagação para animais de contato não infectados e não tratados, que foram coalojados com furões infectados e tratados.
 Ciência e Saúde
Ciência e Saúde
 Ciência e Saúde
Ciência e Saúde
 Ciência e Saúde
Ciência e Saúde
 Ciência e Saúde
Ciência e Saúde