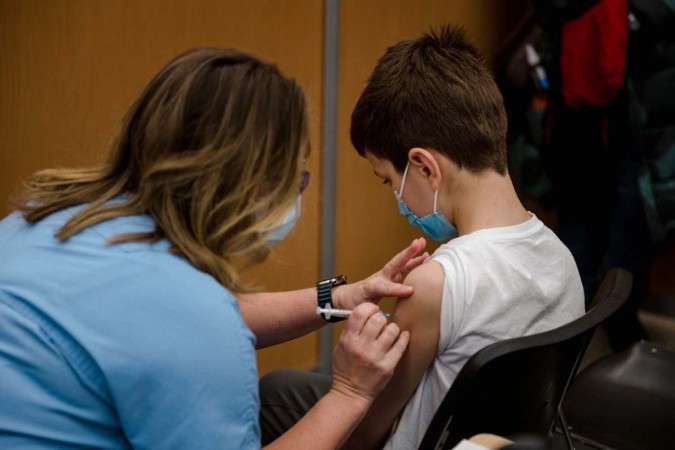
A Agência Nacional de Vigilância Sanitária (Anvisa) concluiu a avaliação técnica sobre o pedido de autorização para aplicação da vacina contra a covid-19 da Pfizer, a Comirnaty, para crianças de 5 a 11. O resultado da análise será divulgado nesta quinta (16/12) em reunião virtual com a presença das áreas técnicas da agência.
"A finalização da análise ocorre após a submissão à agência de dados complementares pela desenvolvedora", informou a Anvisa nesta quarta (15). Além do corpo técnico do órgão regulador, a avaliação do pedido da Pfizer contou com a participação de representantes de sociedades médicas brasileiras, como a Sociedade Brasileira de Pediatria (SBP), entre outras.
A participação desses especialistas na análise da autorização da vacina para crianças tem caráter consultivo. A Pfizer solicitou à agência a autorização para a aplicação da vacina contra a covid-19 em crianças em 12 de novembro. O imunizante da farmacêutica já tem registro definitivo no Brasil para aplicação em pessoas com mais de 12 anos e é aplicado no Brasil neste público-alvo.
Agora, a Pfizer visa ampliar o público-alvo do imunizante contra a covid-19. Vale lembrar que a apresentação, os ingredientes e a dosagem da vacina Comirnaty para crianças de 5 a 11 anos são diferentes da vacina para adultos.
"O anúncio da avaliação técnica e resultado será em reunião virtual a partir das 10h30", informou a Anvisa.
CoronaVac
Em agosto, a Diretoria Colegiada da Anvisa, por unanimidade, considerou que ainda não era seguro aprovar o uso da CoronaVac em crianças a partir de 3 anos até adolescentes com 17 anos. O uso da vacina na população adulta já foi aprovado pela Anvisa.
No início de dezembro, o Instituto Butantan, produtor da CoronaVac no Brasil, informou que enviará para a agência reguladora nova solicitação de uso da vacina em crianças. Segundo o diretor do Instituto, Dimas Covas, a entrega da documentação à Anvisa deveria acontecer ainda nesta semana.
Dessa forma, o governo do estado de São Paulo reservou 12 milhões de doses da CoronaVac com o objetivo de aplicar o imunizante em crianças de 3 a 11 anos, a partir da autorização do órgão regulador.
Saiba Mais
-
![]() Mundo
Vacina da Johnson & Johnson pode ser usada como dose de reforço, afirma agência europeia
Mundo
Vacina da Johnson & Johnson pode ser usada como dose de reforço, afirma agência europeia
-
![]() Brasil
Anvisa amplia ações para verificar comprovação vacinal em fronteiras
Brasil
Anvisa amplia ações para verificar comprovação vacinal em fronteiras
-
![]() Política
Bolsonaro entrega PCR negativo e confirma presença na posse de Mendonça no STF
Política
Bolsonaro entrega PCR negativo e confirma presença na posse de Mendonça no STF
-
![]() Cidades DF
Dose de reforço da Janssen começa a ser aplicada em professores
Cidades DF
Dose de reforço da Janssen começa a ser aplicada em professores
Notícias pelo celular
Receba direto no celular as notícias mais recentes publicadas pelo Correio Braziliense. É de graça. Clique aqui e participe da comunidade do Correio, uma das inovações lançadas pelo WhatsApp.
Dê a sua opinião
O Correio tem um espaço na edição impressa para publicar a opinião dos leitores. As mensagens devem ter, no máximo, 10 linhas e incluir nome, endereço e telefone para o e-mail sredat.df@dabr.com.br.
 Mundo
Mundo
 Brasil
Brasil
 Política
Política
 Cidades DF
Cidades DF